Știri
De ce scade capacitatea bateriilor de tip litiu-ion?
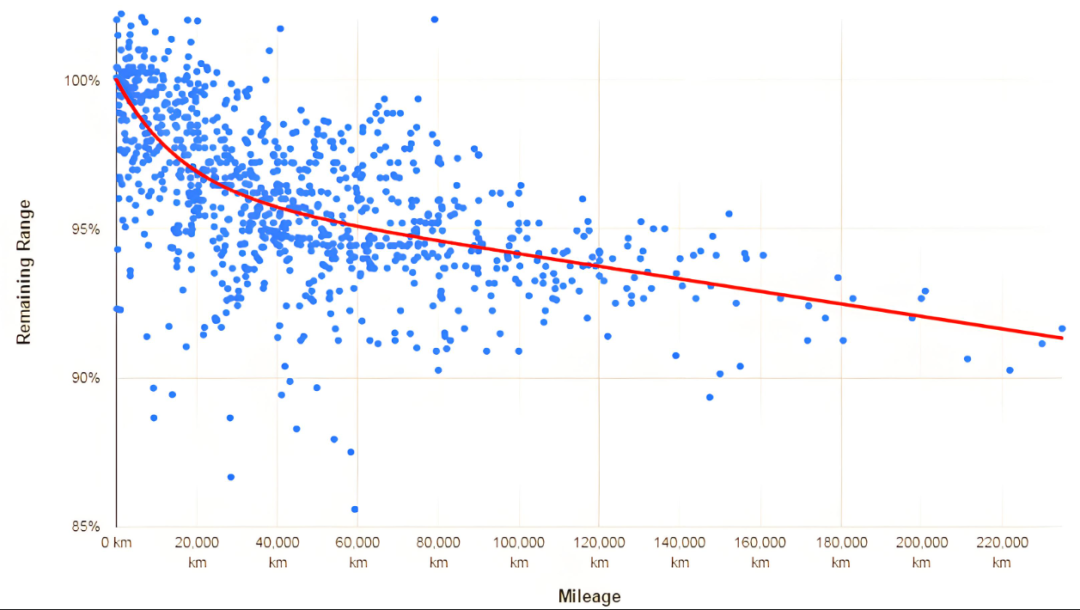
Baterii litiu-ion degradarea capacității se referă la fenomenul prin care bateriile litiu-ion își pierd treptat capacitatea disponibilă în timp și odată cu durata de viață a bateriei. Care este mecanismul degradării capacității?
1. Modificarea volumului
În timpul procesului de încărcare și descărcare a bateriei, ionii de litiu se intercalează și se deintercalează, provocând extinderea/contractarea rețelelor materialelor de electrozi pozitivi și negativi într-o măsură variabilă.
A. Microstructura materialului catodic se modifică, determinând o scădere a cantității de litiu intercalat. În condiții de suprancărcare, ionii de litiu migrează rapid spre anod, provocând colapsul rețelei catodice.
B. Modificarea volumului grafitului de la electrodul negativ în timpul intercalării și deintercalării ionii de litiu poate atinge 10%, determinând stratificarea particulelor.
2. Formarea filmului SEI
În timpul fazei de formare a bateriei, ionii de litiu reacționează chimic cu anumite componente ale electrolitului în timpul procesului inițial de încărcare și descărcare, formând o interfață solidă de electrolit ireversibilă la interfața dintre electrodul negativ și electrolit. În timpul procesului de încărcare și descărcare, SEI se degradează continuu și se regenerează, ceea ce duce la o scădere a ionilor de litiu activi, o creștere a grosimii filmului SEI și o creștere a rezistenței interne.
3. Creșterea dendritelor de litiu
În condiții de temperatură scăzută, încărcare rapidă și suprancărcare, ionii de litiu continuă să se deplaseze către electrodul negativ. Rata de extracție a ionilor de litiu este mai mare decât rata de încorporare a acestora, ceea ce duce la depunerea ionilor de litiu în apropierea electrodului negativ și la reducerea litiului activ.
4. Descompunerea electrolitului
Descompunerea electrolitului are loc în principal prin două căi: descompunere electrochimică și descompunere chimică. Descompunerea electrochimică este împărțită în descompunere oxidativă pe partea electrozilor pozitivi și descompunere reductivă pe partea electrozilor negativi. Descompunerea oxidativă pe partea electrozilor pozitivi apare atunci când potențialul electrozilor pozitivi este >4,5 V, provocând umflarea bateriei și creșterea impedanței interfaciale. Descompunerea reductivă pe partea electrozilor negativi apare atunci când potențialul electrozilor negativi din grafit este <0,8 V, determinând îngroșarea stratului SEI al bateriei și reducerea litiului activ. Descompunerea chimică este împărțită în reacții catalizate de urme de apă și reacții de descompunere la temperatură ridicată. Reacțiile catalizate de urme de apă provoacă corodarea electrozilor pozitivi. Reacțiile de descompunere la temperatură ridicată determină uscarea electrolitului, ducând la tendința de răspuns termic necontrolat.
5. Coroziunea colectorului de curent
Coroziunea colectorului de curent este clasificată ca fiind coroziunea foliei de aluminiu de la electrodul pozitiv la un potențial ridicat și coroziunea foliei de cupru de la electrodul negativ la un potențial scăzut. Atunci când potențialul electrodului pozitiv depășește 3,8 V, folia de aluminiu de la electrodul pozitiv se oxidează și corodează. În condiții de suprancărcare, atunci când potențialul electrodului negativ este mai mic de 3 V, folia de cupru se dizolvă, migrează către electrodul pozitiv și se depune pe suprafața acestuia.
Există, de asemenea, defectarea agenților conductori și îmbătrânirea diafragmelor.


