חדשות
מדוע יורד הקיבולת של סוללות ליתיום-יון?
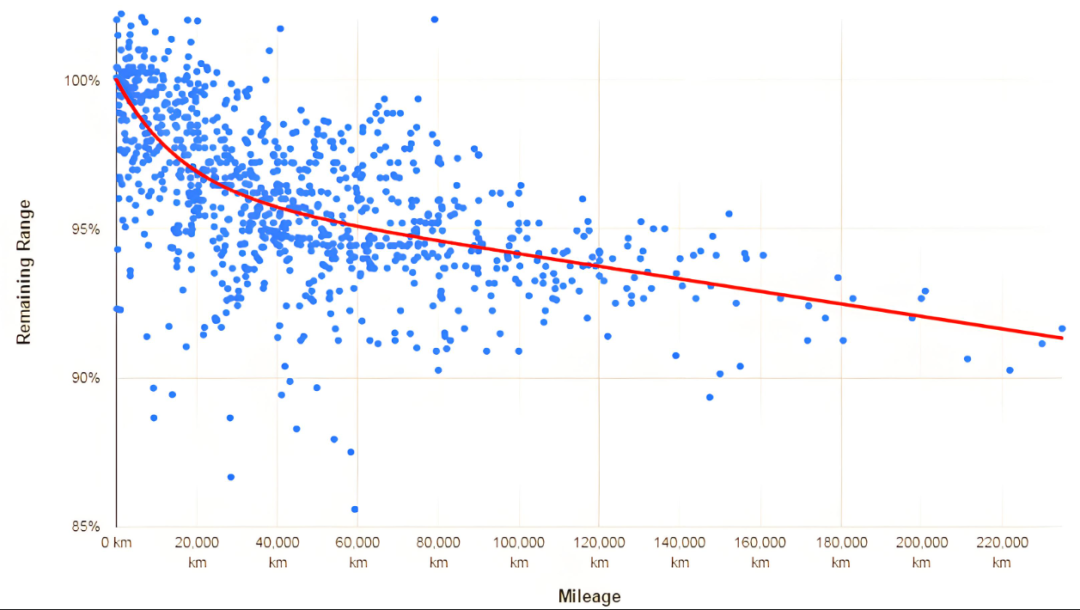
תא ליתיום-יון דעיכת קיבולת מציינת את התופעה לפיה סוללות ליתיום-יון מאבדות בהדרגה את הקיבולת הזמינה שלהן עם הזמן ועל פני חיי הסוללה. מהו המנגנון של דעיכת הקיבולת?
1. שינוי נפח
במהלך תהליך טעינה ופריקה של הסוללה, יוני הליתיום מתקנים ומתרחקים מהאלקטרודות, מה שגורם לרשתות של חומרי האנודה והקתודה להתרחב ולצמצם במידה שונה.
א. המבנה המיקרוסקופי של חומר הקתודה משתנה, מה שמביא לירידה בכמות הליתיום שנכנס. בתנאי טעינה יתר, יוני הליתיום migru במהירות לאנודה, מה שגורם לרשת הקתודה להתפורר.
ב. שינוי הנפח של הגרפיט באנודה במהלך הכנסת והוצאת יונים של ליתיום יכול להגיע ל-10%, מה שמביא לשכבת חלקיקים.
2. היווצרות שכבת SEI
במהלך שלב היווצרות הסוללה, יוני הליתיום מגיבים כימית עם רכיבים מסוימים של האלקטרוליט במהלך תהליך הטעינה והפריקה הראשוני, וсоздים ממשק אלקטרוליט מוצק בלתי הפיך בממשק בין האלקטרודה השלילית לאלקטרוליט. במהלך תהליך הטעינה והפריקה, שכבת ה-SEI נשברת ומבוצרת שוב ושוב, מה שגורם לירידה בכמות יוני הליתיום הפעילים, עלייה בעובי שכבת ה-SEI ועלייה בהתנגדות הפנימית.
3. צמיחה של צינורות ליתיום
בתנאי טמפרטורה נמוכה, טעינה מהירה וטעינה מוגזמת, יוני הליתיום ממשיכים לנוע לכיוון האלקטרודה השלילית. קצב הוצאה של יוני הליתיום גבוה מקצב השיכון שלהם, מה שגורם להיצטברות יוני הליתיום ליד האלקטרודה השלילית וצמצום הכמות הפעילות של הליתיום.
4. פירוק האלקטרוליט
פירוק האלקטרוליט מתרחש בעיקר בשתי דרכים: פירוק אלקטרוכימי ופירוק כימי. פירוק אלקטרוכימי מחולק לפירוק חמצוני בצד האלקטרודה החיובית ופירוק מוחלט בצד האלקטרודה השלילית. פירוק חמצוני בצד האלקטרודה החיובית מתרחש כאשר הפוטנציאל של האלקטרודה החיובית הוא גבוה מ-4.5 וולט, מה שגורם לבליטה בבattery ולעלייה בהתנגדות הבין-פזית. פירוק מוחלט בצד האלקטרודה השלילית מתרחש כאשר הפוטנציאל של האלקטרודה השלילית הגרפיטית הוא נמוך מ-0.8 וולט, מה שגורם לשכבת ה-SEI של הסוללה לה Gros ופחתת את הליתיום הפעיל. פירוק כימי מחולק לתגובות שזרות מים קטלזיות ותגובת פירוק בטמפרטורה גבוהה. תגובות שזרות מים קטלזיות גורמות לאיטום האלקטרודה החיובית. תגובות פירוק בטמפרטורה גבוהה גורמות לאיבוד האלקטרוליט, מה שמוביל לנטייה לפריצת חום.
5. קורוזיה של אוסף הזרם
קורוזיה של אוגרי הזרם מסווגת כקורוזיה של פוליאלומיניום באלקטרודה החיובית בפוטנציאל גבוה וקורוזיה של פולי נחושת באלקטרודה השלילית בפוטנציאל נמוך. כאשר פוטנציאל האלקטרודה החיובית עולה על 3.8V, פוליאלומיניום באלקטרודה החיובית מתחמצן ומת corroded. בתנאי טעינה מוגזמת, כאשר פוטנציאל האלקטרודה השלילית נמוך מ-3V, פולינחושת נמסה, עוברת לאלקטרודה החיובית, ומשקעת על פני השטח של האלקטרודה החיובית.
ישנם גם כשלים של agents מוליכים וشيخוּת של מפרידים.


