Новини
Защо капацитетът на литиево-йонните батерии намалява?
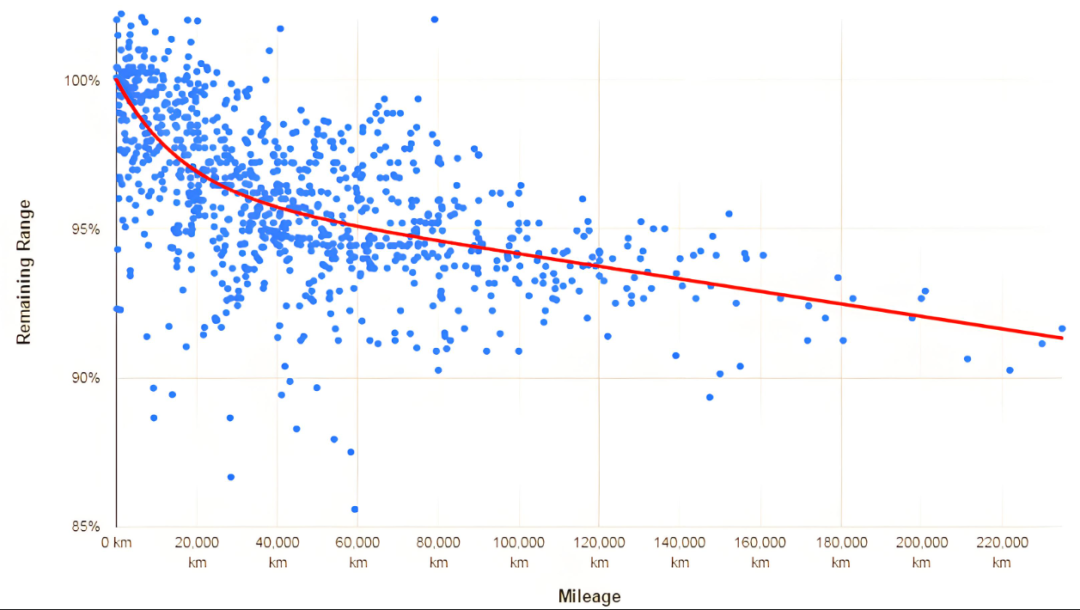
Литиево-ионна батерия способността на батериите от литиев тип да съхраняват енергия намалява с времето и с използването им. Какъв е механизъмът на това намаляване на капацитета?
1. Промяна в обема
По време на процеса на зареждане и изтощване на батерията, литиевите йони се вмъкват и извличат, което предизвиква разширване/свиване на структурата на положителните и отрицателните електродни материали в различна степен.
A. Микроструктурата на катодния материал се променя, което води до намаляване на количеството внедрени литиеви йони. При прекомерно зареждане, литиевите йони бързо се преместват към анода, което предизвиква срутване на катодната решетка.
B. Обемната промяна на графита в отрицателния електрод по време на внедряване и извличане на йони на литий може да достигне 10%, което води до слоестост на частиците.
2. Формиране на SEI филм
По време на фазата на формиране на батерията, йоните на литий химически реагират с определени компоненти на електролита по време на процеса на първоначално зареждане и изтощване, като се формира необратим твърд електролитен интерфейс на границата между отрицателния електрод и електролита. По време на процеса на зареждане и изтощване, SEI непрекъснато се разрушава и регенерира, което води до намаляване на активните йони на литий, увеличаване на дебелината на SEI филма и увеличаване на вътрешното съпротивление.
3. Растеж на литиеви дендрити
При ниска температура, бързо зареждане и прекомерно зареждане, йоните на литий продължават да се движат към отрицателния електрод. Скоростта на екстракция на йони на литий е по-голяма от скоростта на внедряване на йони на литий, което води до отлагане на йони на литий в близост до отрицателния електрод и намаляване на активния литий.
4. Разлагане на електролита
Електролитната дисоциация протича предимно по два начина: електрохимична дисоциация и химична дисоциация. Електрохимичната дисоциация се разделя на окислителна дисоциация от страната на положителния електрод и редукционна дисоциация от страната на отрицателния електрод. Окислителната дисоциация от страната на положителния електрод настъпва, когато потенциалът на положителния електрод е >4.5V, което причинява издуване на батерията и увеличаване на междинното съпротивление. Редукционната дисоциация от страната на отрицателния електрод настъпва, когато потенциалът на графитния отрицателен електрод е <0.8V, което води до уплътняване на SEI слоя на батерията и намаляване на активния литий. Химичната дисоциация се разделя на реакции, катализирани от следи вода, и реакции на дисоциация при висока температура. Реакциите, катализирани от следи вода, причиняват корозия на положителния електрод. Реакциите на дисоциация при висока температура причиняват изсъхване на електролита, което води до склонност към топлинен удар.
5. Корозия на токопроводящия електрод
Корозията на токоприемника се класифицира като корозия на алуминиевата фолия на положителния електрод при висок потенциал и корозия на медната фолия на отрицателния електрод при нисък потенциал. Когато потенциалът на положителния електрод надвиши 3,8 V, алуминиевата фолия на положителния електрод се окислява и корозира. При условия на пренапрежение, когато потенциалът на отрицателния електрод е по-малък от 3 V, медната фолия се разтваря, мигрира към положителния електрод и се отлага на повърхността на положителния електрод.
Съществуват също така повреди на проводящите агенти и стареене на диафрагмите.


